(1R,3S,4S)-3-(6-溴-1H-苯并咪唑-2-基)-2-氮杂双环[2.2.1]庚烷-2-羧酸叔丁酯的制备方法
背景及概述[1]
(1R,3S,4S)-3-(6-溴-1H-苯并咪唑-2-基)-2-氮杂双环[2.2.1]庚烷-2-羧酸叔丁酯可用作医药合成中间体,如制备新抗病毒NS5A抑制剂Ledipasvir(GS5885)与NS5B阻断剂Sofosbuvir二联复方组合的Harvoni,是吉利德2013年12月获准的一个重磅丙肝治疗药物。Harvoni是第一个批准用于治疗基因1型丙肝感染,且不需要联合干扰素或利巴韦林的全口服抗丙肝方案。Harvoni既可以单药使用,也可以和其它口服制剂比如利巴韦林联合使用。
制备[1]
(1R,3S,4S)-3-(6-溴-1H-苯并咪唑-2-基)-2-氮杂双环[2.2.1]庚烷-2-羧酸叔丁酯采用以下步骤合成得到:
步骤S1:按照以下合成路线先得到化合物2;

取4.0g2-溴芴加入,分散于175mL冰醋酸中,加入20%硫酸16mL,碘酸钾0.7g,单质碘2.24g,于80℃下加热反应24小时。关闭加热,冰浴冷却反应,加冷水165mL稀释反应混合物,抽滤,滤饼用自来水洗至滤液无色。收集所得固体,60℃真空干燥过夜,加3:1(体积比)的二氯甲烷和甲醇混合物40mL,60℃油浴加热下搅拌打浆1小时,自然冷却过夜,抽滤,固体真空60℃真空干燥过夜得化合物2为白色固体(4.37g)。
1HNMR(75MHz,DMSO)δ7.98(s,1H),7.87(s,1H),7.80(s,1H),7.75(d,J=0.8Hz,2H),7.58(dd,J=8.2,1.8Hz,1H),3.95(s,2H)。
步骤S2:按照以下合成路线先得到化合物4;
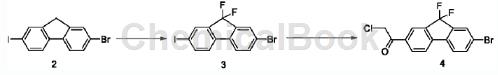
取化合物21.96g,并将N-氟代双本磺酰胺6.66g在氮气保护下加入到40mL无水四氢呋喃溶解,冰盐浴冷却30分钟,之后在20分钟内滴加双三甲基硅胺基钾(1M的四氢呋喃溶液),滴加完毕自然升温反应3h。冰浴冷却反应液,滴加0.1mL甲醇(试剂级),加入正己烷40mL稀释反应液。以上混悬液搅拌30分钟后过滤,滤饼用石油醚(50mLx3)洗涤,收集滤液浓缩,柱层析(石油醚)得化合物3米白色固体(2.57g)。取化合物32.48g在氮气保护下加20mL无水四氢呋喃溶解,冰盐浴冷却搅拌10分钟。量取3.4mL异丙基氯化镁四氢呋喃溶液(2M)于5分钟内滴加到以上溶液中,搅拌反应27分钟,之后滴加N-甲基-N-甲氧基-2-氯乙酰胺的甲苯溶液(0.92g溶于8mL无水甲苯)。滴加完毕继续在冰盐浴冷却下反应15分钟,撤除冰盐浴,自然升温反应4小时,TLC显示反应完毕(PE:EA5/1,RF值0.3)。向反应液中滴加4N盐酸调pH到1-2左右,加甲基叔丁基醚20mL,饱和食盐水20mL,震荡分液。有机相用无水硫酸镁干燥5分钟过滤,浓缩蒸干四氢呋喃与甲基叔丁基醚,所得油状物加正己烷-二氯甲烷(20:1,22mL)于70℃油浴锅中加热搅拌回流30分钟,之后自然冷却至室温,过滤,滤饼用冷正己烷(5mLx3)洗涤,真空干燥得化合物4为淡黄色固体(1.51g)。
1HNMR(75MHz,CDCl3)δ8.19(d,J=1.1Hz,1H),8.13(d,J=8.0Hz,1H),7.82(d,J=1.5Hz,1H),7.68(d,J=8.4Hz,2H),7.53(d,J=8.1Hz,1H),4.72(s,2H)。
步骤S3:按照以下合成路线先得到化合物7;

取1.44g化合物4,并加入0.98g脯氨酸衍生物5、碘化钾66mg,加20mL乙腈室温搅拌分散均匀,加入二异丙基乙基胺540mg,室温搅拌反应5小时,点板显示反应完毕。减压蒸干反应液,加20mL乙酸乙酯溶解所得油状物,先后用1N盐酸,5%氢氧化钠水溶液和饱和食盐水洗,有机相用无水硫酸镁-无水硫酸钠干燥,过滤浓缩蒸干得到化合物6的粗品为褐色油状物。加25mL甲苯溶解以上所得6的粗品,加入醋酸铵6.2g,氮气保护下于95℃油浴锅中加热搅拌反应过夜,撤除油浴,冰浴冷却反应,加乙酸乙酯10mL稀释,先后用水(20mL)、5%的碳酸氢钠(20mL)、饱和食盐水洗。分液,有机相用无水硫酸钠-无水硫酸镁干燥,减压蒸干,加15ml乙酸乙酯搅拌回流30分钟,趁回流滴加正己烷15mL,之后搅拌自然降温至室温,过滤,滤饼用乙酸乙酯-正己烷(1:5,5mLx3)洗,真空干燥过夜得产物7为棕色粉末状固体(1.32g)。
1HNMR(75MHz,CDCl3)δ10.61(s,1H),8.01(s,1H),8.01(s,1H),8.01(s,1H),7.89(d,J=7.7Hz,1H),7.74(d,J=1.3Hz,1H),7.57(d,J=8.1Hz,1H),7.50(d,J=7.6Hz,1H),7.40(d,J=7.9Hz,1H),7.31(s,1H),5.11(d,J=6.0Hz,1H),3.51(d,J=10.3Hz,1H),3.13(d,J=10.3Hz,1H),2.82(d,J=12.3Hz,1H),2.35(t,J=10.5Hz,1H),1.50(s,9H),0.90(s,1H),0.75–0.49(m,3H)。
步骤S4:按照以下合成路线先得到化合物12;
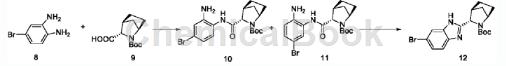
取化合物8(768mg),化合物9(890mg),加15mLN,N-二甲基甲酰胺室温搅拌溶解,先后加入N-甲基吗啡啉(830mg)和2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(HATU,1.71g),室温反应。1小时后向反应液中加水150mL,乙酸乙酯萃取(25mLx3),食盐水洗有机相,无水硫酸镁-无水硫酸钠干燥减压蒸干溶剂得到10和11的混合物为红褐色油状物。以上油状物加20mL无水乙醇溶解,115℃油浴锅中封管加热反应48小时。蒸干乙醇,柱层析(石油醚-乙酸乙酯,2:1)纯化得化合物12为黄褐色油状或泡沫状固体(1.59g)。
1HNMR(75MHz,CDCl3)δ10.72(s,1H),7.59(dd,J=10.9,5.1Hz,1H),7.45–7.19(m,2H),4.54(d,J=2.6Hz,1H),4.17(s,1H),3.45(d,J=3.4Hz,1H),2.05–1.7(m,6H),1.54
主要参考资料
[1] (CN106117187) 一种丙型肝炎病毒抑制剂、药物组合物及其应用
你可能感兴趣的
- 亨斯迈钛白粉
- 巴斯夫抗氧剂
- 巴斯夫颜料染料
- 科莱恩颜料染料
- 朗盛颜料
- 纽碧莱颜料
- 好利得颜料
- 卡博特色母粒
- 陶氏杀菌剂
- 罗门哈斯阻垢剂
- 三菱大孔树脂
- 卡博特白炭黑
- 信越硅油
- 道康宁硅油
- 杜邦钛白粉
- 伊士曼纤维素
- 巴斯夫高岭土
- 英格瓷高岭土
- 雅宝抗氧剂
- 抗氧剂
- 长春抗氧剂
- 道康宁硅胶
- GE迈图硅胶
- 安泰密封胶
- 爱卡颜料
- 默克珠光颜料
- 科莱恩抗氧剂
- 特诺钛白粉
- 瓦克VAE乳液
- 特密高碳黑
- 百合花颜料
- 朗盛橡胶
- 陶氏增韧剂
- 华乐荧光颜料
- 陶氏胶粘剂
- 艾迪科抗氧剂
- 利安隆抗氧剂
- 韩国三华色母粒
- 德固赛消光粉
- 三菱碳黑
- 卡博特碳黑
- 德固赛碳黑
- 德固赛白炭黑
- 瓦克白炭黑
- 德山白炭黑
- 科莱恩蜡粉
- 霍尼韦尔蜡粉
- 巴斯夫蜡粉
- 白炭黑
- 碳黑
【版权声明】秉承互联网开放、包容的精神,凯茵化工欢迎各方(自)媒体、机构转载、引用我们原创内容,但要严格注明来源凯茵化工;同时,我们倡导尊重与保护知识产权,如发现本站文章存在版权问题,烦请将版权疑问、授权证明、版权证明、联系方式等,发邮件至 app@shkingchem.com,我们将第一时间核实、处理。














